HISTÓRICO – Aprueban el primer fármaco que puede retrasar por años la diabetes tipo 1
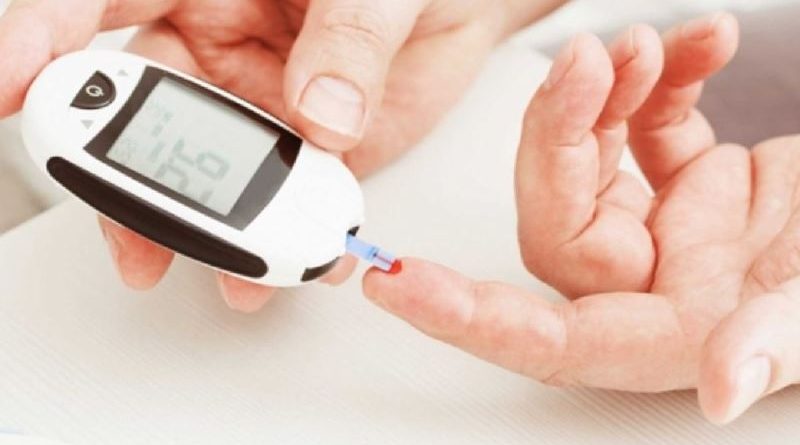
La Administración de Alimentos y Medicamentos (FDA) aprobó el primer tratamiento que puede retrasar – posiblemente durante años – la aparición de la diabetes tipo 1, enfermedad que suele aparecer en los adolescentes.
El nuevo fármaco, teplizumab, es fabricado por Provention Bio, que se asociará con Sanofi para comercializar el medicamento en Estados Unidos bajo la marca Tzield.
Clarín consultó a Sanofi sobre si hay planes para que el medicamento sea comercializado en Argentina. Respondieron que la sociedad del laboratorio con Provention Bio es «sólo para Estados Unidos».
En una llamada en conferencia con inversores el viernes, Provention dijo que el vial del medicamento costaría 13.850 dólares o 193.900 dólares el tratamiento de 14 días. La empresa anunció que el teplizumab debería estar disponible a fin de año.
El fármaco, que la FDA aprobó el jueves pasado, no cura ni previene la diabetes tipo 1 sino que demora su aparición un promedio de dos años y, en el caso de algunos pacientes afortunados, mucho más.
Hasta ahora la demora más larga fue de 11 años, dijo Kevan Herold, de Yale, investigador principal de los ensayos del medicamento.
El único otro tratamiento para la enfermedad -la insulina- se descubrió hace cien años y no afecta al curso de la enfermedad. Sólo reemplaza lo que falta.
El teplizumab se utilizará para tratar a pacientes con alto riesgo de padecer diabetes tipo 1 que presenten anticuerpos indicadores de un ataque inmunitario al páncreas y cuya tolerancia a la glucosa no sea normal.
El tratamiento consiste en una infusión intravenosa de 14 días del fármaco, un anticuerpo monoclonal que bloquea los linfocitos T, impidiendo que ataquen las células productoras de insulina del páncreas.
«Hable con cualquier persona que tenga diabetes tipo 1 y cualquier día que no esté agobiado por medir el azúcar en sangre cuatro veces diarias e inyectarse insulina es un día glorioso», dijo Mark S. Anderson, director del centro de diabetes de la Universidad de California en San Francisco e investigador del ensayo clínico fundamental que llevó a la aprobación del tratamiento.
John Buse, experto en diabetes de la Universidad de Carolina del Norte, que no participó en el estudio, calificó la aprobación de «muy emocionante» y dijo que «pondría patas arriba el mundo de la diabetes tipo 1.» «Siempre ha existido la idea de que el screening o cribado sería una buena idea», dijo. Pero los expertos médicos «nunca lo han promovido para detectar la diabetes tipo 1».
Eso no será fácil: ninguna prueba de cribado lo es. Pero en este caso, muy pocos de los que se sometan a los tests padecerán esta rara pero nefasta enfermedad, que sólo afecta a cuatro de cada 1.000 personas de la población general.
La diabetes tipo 1 suele aparecer en la adolescencia, cuando los pacientes repentinamente empiezan a sentirse cansados todo el tiempo, orinan con frecuencia, beben grandes cantidades de agua y pierden peso.
Con el diagnóstico de diabetes, su vida cambia por completo. Tienen que medirse el azúcar en sangre y administrarse insulina durante el resto de su vida. Cada vez que comen, tienen que calcular la cantidad de insulina que necesitan.
También se enfrentan al fantasma de las complicaciones: enfermedades de los ojos que pueden provocar ceguera, insuficiencia renal, problemas cardíacos y accidentes cerebrovasculares. Sin un buen control de la glucosa en sangre, las complicaciones pueden aparecer ya a los cinco años después del diagnóstico, dijo Anderson.
El nuevo tratamiento, agregó Anderson, «abre la puerta», de forma similar a cómo la primera inmunoterapia para el cáncer supuso un avance hacia una nueva era de tratamiento hace una década. Espera que, conforme la inmunoterapia para la diabetes mejore, se pueda detener la enfermedad antes de que se instale.
El nuevo fármaco no es un tratamiento para el tipo de diabetes mucho más común, el tipo 2, en el que el páncreas produce insulina pero las células del cuerpo no responden a ella.
La historia del nuevo tratamiento se remonta a los años 80 y en ella participaron investigadores decididos que insistían en la idea a medida que una empresa tras otra -cuatro en total antes de Provention- mostraban interés, pero acababan abandonando el fármaco por diversas razones.
Jeffrey Bluestone, que fue académico hasta hace poco y que ahora es CEO de Sonoma Biotherapeutics, dijo que él y su colega Herold, que fue consultor de Provention y otras empresas, pasaron veinte años «tratando de mantener vivo el medicamento».
«A los científicos los entusiasmaba», dijo Bluestone, que es consultor de Provention y miembro del consejo de administración de la empresa. «A la gente de las empresas les apasionaba». Pero, por razones ajenas a su potencial, lo abandonaban una y otra vez.
Herold dijo que recordaba vívidamente los viajes que él, Bluestone y una investigadora francesa, Lucienne Chatenoud, de la Universidad Descartes de París, hicieron a las compañías farmacéuticas «rogándoles que no abandonaran el fármaco».
En un momento dado, Bluestone tomó el anticuerpo, desarrollado entonces por Ortho Pharmaceuticals, y produjo un lote clínico del medicamento en el laboratorio. Herold lo probó en un pequeño estudio con personas con un diagnóstico reciente de diabetes tipo 1.
El tratamiento extendió el periodo en el que generaban algo de insulina, pero finalmente todos tuvieron diabetes.
En 2011, Bluestone y Herold propusieron un tipo de estudio diferente. Tratarían a personas con alto riesgo de diabetes pero que aún no la padecían. Fue una decisión audaz, señaló Bluestone. «Aparte de las vacunas, no hay muchos medicamentos que se administren antes del diagnóstico», dijo.
Para encontrar a las personas, los investigadores trabajaron con un grupo de centros de ensayos clínicos, TrialNet, que contaba con el apoyo de los Institutos Nacionales de Salud (NIH). Herold es ahora presidente del grupo. Los investigadores de TrialNet examinaron a 200.000 personas que eran familiares directos de pacientes con diabetes tipo 1, en busca de anticuerpos que indicaran un ataque inmunitario al páncreas y un metabolismo anormal de la glucosa.
El resultado fue un estudio, publicado en The New England Journal of Medicine, que llevó a la aprobación del jueves.
Ahora que el fármaco está aprobado, el reto será encontrar a las personas que puedan beneficiarse. Si sólo se examina a las personas con familiares directos que tienen diabetes, se perderá al 85% de los pacientes.
JDRF, una agrupación sin fines de lucro que aboga por las personas con diabetes tipo 1 y apoya la investigación y que, junto con los NIH, financió el ensayo que condujo a la aprobación del fármaco, quiere que las pruebas de detección de anticuerpos formen parte de la atención pediátrica de rutina.
«La mayoría de las familias dicen que el diagnóstico cae como un rayo», dijo Aaron Kowalski, director general de JDRF. Y la mayoría de los pacientes, añadió, ya están muy enfermos cuando se los diagnostica por primera vez.
La agrupación ha realizado análisis de sangre para buscar anticuerpos en Alemania y algunas zonas de Colorado. Y ofrece un test casero que se puede solicitar, financiado por la fundación. Pero, dijo Kowalski, «queremos que los consultorios pediátricos lo hagan».
Los testeos también ofrecen otra oportunidad, dijo. Resulta que los anticuerpos que revelan un ataque inmunitario suelen aparecer cuando las personas tienen tan sólo 5 o 6 años, aunque la mayoría no desarrolla la diabetes hasta la adolescencia.
Ahora, dijo, su esperanza es tratar a las personas incluso antes, tan pronto como surjan esos anticuerpos. Los médicos y la FDA se habían opuesto anteriormente a dar tratamiento antes de que la enfermedad estuviera claramente en marcha y se preguntaban: «¿Cómo puede darse inmunoterapia si son normales?», explicó Kowalski.
Sin embargo, los anticuerpos cuentan otra historia.
«Sí tienen diabetes», dijo, aunque no según la definición habitual de la enfermedad. «Sólo que aún no se ha desenmascarado. Tenemos que ayudarlos a salvar sus células beta», las células secretoras de insulina del páncreas.
Herold es prudente. Si alguien tiene anticuerpos pero su páncreas no está siendo atacado activamente, el tratamiento puede no servir.
«Es difícil detener algo que no está sucediendo», dijo.
Bluestone y Herold se preguntan si la administración de una segunda ronda de tratamiento podría mejorar aún más los resultados.
Por ahora, a Bluestone le gustaría que el tratamiento se utilizara para ayudar a pacientes más jóvenes que los que participaron en el ensayo. Está aprobado para pacientes de al menos 8 años de edad. «Pero la enfermedad afecta a muchos pacientes de menos de 8 años», dijo.
Aunque él y otros están entusiasmados con la posibilidad de prevenir algún día la enfermedad por completo, los expertos en diabetes tienen ante sí un desafío inmediato.
«Lo más importante en este momento es encontrar a los posibles pacientes», dijo Bluestone.
The New York Times. Especial – CLARIN